Covid-19-Infektion kann Gefäßschäden im Herz verursachen
Autor: Tom Wannenmacher
Wir brauchen deine Hilfe – Unterstütze uns!
In einer Welt, die zunehmend von Fehlinformationen und Fake News überflutet wird, setzen wir bei Mimikama uns jeden Tag dafür ein, dir verlässliche und geprüfte Informationen zu bieten. Unser Engagement im Kampf gegen Desinformation bedeutet, dass wir ständig aufklären und informieren müssen, was natürlich auch Kosten verursacht.
Deine Unterstützung ist jetzt wichtiger denn je.
Wenn du den Wert unserer Arbeit erkennst und die Bedeutung einer gut informierten Gesellschaft für die Demokratie schätzt, bitten wir dich, über eine finanzielle Unterstützung nachzudenken.
Schon kleine Beiträge können einen großen Unterschied machen und helfen uns, unsere Unabhängigkeit zu bewahren und unsere Mission fortzusetzen.
So kannst du helfen!
PayPal: Für schnelle und einfache Online-Zahlungen.
Steady: für regelmäßige Unterstützung.

Ein interdisziplinäres Forschungsteam der Universitäten Göttingen und der Medizinischen Hochschule Hannover (MHH) hat wesentliche Veränderungen im Herzmuskelgewebe von Menschen nachgewiesen, die an Covid-19 gestorben sind.
Nachdem die Schädigung von Lungengewebe schon seit längerem im Fokus der Wissenschaft steht und inzwischen gut erforscht ist, untermauert die aktuelle Studie die Beteiligung des Herzens bei Covid-19 erstmals auf zellulärer Ebene durch eine Visualisierung und Analyse des betroffenen Gewebes in der dritten Dimension. Die Ergebnisse sind in der Fachzeitschrift eLife erscheinen.
Die Wissenschaftlerinnen und Wissenschaftler bildeten die Gewebearchitektur mittels Synchrotronstrahlung – einer besonders brillanten Röntgenstrahlung – mit hoher Auflösung ab und stellten sie dreidimensional dar. Dazu nutzten sie ein spezielles Röntgenmikroskop, das die Universität Göttingen am Deutschen Elektronensynchrotron DESY in Hamburg errichtet hat und betreibt. In den untersuchten schweren Krankheitsverläufen von Covid-19 beobachteten sie damit starke Veränderungen auf der Ebene feinster Gefäße, der sogenannten Kapillaren, im Herzmuskelgewebe.
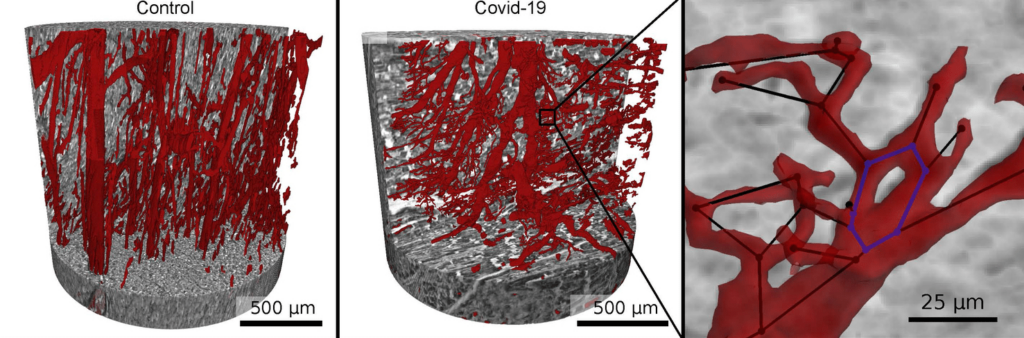
Foto: M. Reichardt, P. Møller Jensen, T. Salditt
Im Vergleich zum gesunden Herzen zeigte sich hier ein durch Neubildung und Aufspaltung der Gefäße chaotisch umgebautes Netzwerk voller Abspaltungen, Verzweigungen und Schlaufen. Diese Veränderungen sind der erste direkte visuelle Nachweis einer speziellen Form der Gefäßneubildung im Gewebe, der sogenannten intussuszeptiven Angiogene, einer der Haupttreiber der Lungenschädigung bei Covid-19. Um das Kapillarnetzwerk zu visualisieren, mussten die Gefäße im dreidimensionalen Volumen mit Methoden des maschinellen Lernens erst identifiziert werden. Dies erforderte zunächst eine aufwendige Markierung der Bilddaten „von Hand“.
„Um die Bildverarbeitung zu beschleunigen, haben wir deshalb die Gewebearchitektur auch automatisiert in ihre lokalen Symmetriemerkmale zerlegt und dann verglichen“, erklärt Erstautor Marius Reichardt von der Universität Göttingen. „Die daraus gewonnenen Parameter zeigten dann im Vergleich zu gesundem Gewebe und Erkrankungen wie schwerer Influenza und gewöhnlicher Herzmuskelentzündung eine völlig andere Qualität“, so die Leiter der Studie, Prof. Dr. Tim Salditt von der Universität Göttingen und Prof. Dr. Danny Jonigk von der MHH.

Foto: M. Reichardt, T. Salditt
Das Besondere an dieser Studie: Im Gegensatz zur Gefäßarchitektur ließ sich die notwendige Datenqualität schon an einer kompakten Röntgenquelle im Labor der Universität Göttingen erreichen – dies könnte im Prinzip auch in jeder Klinik realisiert werden, um Pathologinnen und Pathologen auch in der Routinediagnostik zu unterstützen. Den Ansatz, die charakteristischen Gewebemuster in abstrakte mathematische Auftragungen umzuwandeln, wollen die Forschenden in Zukunft weiter ausbauen, um automatisierte Werkzeuge für die Diagnostik zu entwickeln, wiederum durch die Weiterentwicklung der Labor-Röntgenbildgebung und die Validierung durch Synchrotronstrahlung. Die Zusammenarbeit mit dem DESY wird dazu in den kommenden Jahren weiter ausgebaut.
Originalpublikation:
Marius Reichardt et al. 3D virtual histopathology of cardiac tissue from Covid-19 patients on phase-contrast x-ray tomography. eLife 2021. https://doi.org/10.7554/eLife.71359.
Weitere Informationen:
https://www.uni-goettingen.de/de/3240.html?id=6539 Fotos
FAKE NEWS BEKÄMPFEN
Unterstützen Sie Mimikama, um gemeinsam gegen Fake News vorzugehen und die Demokratie zu stärken. Helfen Sie mit, Fake News zu stoppen!
Mit Deiner Unterstützung via PayPal, Banküberweisung, Steady oder Patreon ermöglichst Du es uns, Falschmeldungen zu entlarven und klare Fakten zu präsentieren. Jeder Beitrag, groß oder klein, macht einen Unterschied. Vielen Dank für Deine Hilfe! ❤️
Mimikama-Webshop
Unser Ziel bei Mimikama ist einfach: Wir kämpfen mit Humor und Scharfsinn gegen Desinformation und Verschwörungstheorien.
Hinweise: 1) Dieser Inhalt gibt den Stand der Dinge wieder, der zum Zeitpunkt der Veröffentlichung aktuell
war. Die Wiedergabe einzelner Bilder, Screenshots, Einbettungen oder Videosequenzen dient zur
Auseinandersetzung der Sache mit dem Thema.
2) Einzelne Beiträge (keine Faktenchecks) entstanden durch den Einsatz von maschineller Hilfe und
wurde vor der Publikation gewissenhaft von der Mimikama-Redaktion kontrolliert. (Begründung)
Mit deiner Hilfe unterstützt du eine der wichtigsten unabhängigen Informationsquellen zum Thema Fake News und Verbraucherschutz im deutschsprachigen Raum
INSERT_STEADY_CHECKOUT_HERE
Kämpfe mit uns für ein echtes, faktenbasiertes Internet! Besorgt über Falschmeldungen? Unterstütze Mimikama und hilf uns, Qualität und Vertrauen im digitalen Raum zu fördern. Dein Beitrag, egal in welcher Höhe, hilft uns, weiterhin für eine wahrheitsgetreue Online-Welt zu arbeiten. Unterstütze jetzt und mach einen echten Unterschied! Werde auch Du ein jetzt ein Botschafter von Mimikama
Mehr von Mimikama
Mimikama Workshops & Vorträge: Stark gegen Fake News!
Mit unseren Workshops erleben Sie ein Feuerwerk an Impulsen mit echtem Mehrwert in Medienkompetenz, lernen Fake News und deren Manipulation zu erkennen, schützen sich vor Falschmeldungen und deren Auswirkungen und fördern dabei einen informierten, kritischen und transparenten Umgang mit Informationen.